健世科技二次递表港交所:核心产品未获批上市短期盈利难 LuX-Valve研发进度领先
出品:新浪财经上市公司研究院
作者:IPO再融资组/辰
历时6个月,健世科技向港交所首次递交的招股材料于2021年12月21日失效,同日健世科技向港交所第二次递表,拟募资用于核心产品LuX-Valve及Ken-Valve生产与商业化、其它在研产品的研发与注册、收购与投资拓展业务、营运资金及一般企业用途。中金公司、花旗担任联席保荐人。
据报道,港股招股书有效期为6个月,因为审计报告有效期届满等各种原因,IPO期间出现上市申请资料失效的情况并不少见,拟发行人可以通过更新资料重新申请“一键激活”上市程序。招股书失效不等于上市失败,也与公司经营情况无直接相关。
截至12月21日,今年在港交所主板递表的企业为356家,其中168家IPO材料正在处理中,62家已上市,4家已撤回,122家招股材料为失效状态。受AI医疗、医疗保健及生物科技等高景气领域企业赴港上市潮和美股转港股上市企业增多的影响,今年港交所招股书失效文件积累较多。
据瑞恩资本统计,扣除重复递表、借壳上市、撤回上市申请的企业,2020年度在港交所主板递表的企业为221家,截至2021年8月15日,通过聆讯131家,通过率59.3%。被拒绝1家,被拒率0.5%。2021年重新递表企业34家,占比15.4%,重新递表的企业分两种情况,一种是6个月失效后重新递表,另一种是失效后再融资然后再递表。
核心产品研发进度领先尚未有产品获批上市
健世科技主打结构性心脏病微创介入,旗下两款核心产品LuX-Valve、Ken-Valve正处于确定性临床试验阶段未获注册。其中LuX-Valve为一款经导管三尖瓣置换(TTVR)系统,适用人群为重度三尖瓣返流且不适合外科手术的高风险患者,优势在于不需要进行常规开胸手术,可以用人工瓣膜支架替代患者具功能障碍的原生三尖瓣的功能。
LuX-Valve为世界首款完成确证性临床试验受试者入组的在研产品,预期将成为全球首批获准商业化的经导管三尖瓣置换产品之一,根据国家药监局的分类标准,LuX-Valve属三类医疗器械。这为其将来的商业化奠定了基础。
但值得注意的是,根据招股书援引CE认证、佛若斯特沙利文分析数据,截至招股书披露日,全球已有三款经导管三尖瓣修复产品获批准,爱德华生命科学旗下Cardioband于2018年获得CE认证,同公司旗下的Pascal于2020年获得CE认证,美国雅培旗下TriClip于2020年获得CE认证。
尽管健世科技旗下LuX-Valve相较于经导管三尖瓣修复产品在患者原生瓣膜情况限制和潜在目标患者群体范围方面拥有较大优势,但两类产品均针对三尖瓣返流同一适应症,产品间存在一定竞争。
另一方面,LuX-Valve虽然是中国唯一一款已知正在处于临床试验阶段的经导管三尖瓣置换在研产品,但在研发进度上面临国际竞争者的紧密追赶。截至招股书披露日,爱德华生命科学旗下的EVOQUE也已进入确定性临床实验阶段,首次发布日距健世科技仅落后一个月左右。
2021年8月,LuX-Valve确证性临床试验受试者入组已经完成,截至招股书披露日,EVOQUE确证性临床试验正进行受试者入组。健世科技能否保持全球领先的研发进度要看临床试验效果如何。
健世科技的另一款核心产品Ken-Valve则是针对重度主动脉瓣返流的一款经导管主动脉瓣置换系统,也属于国家药监局分类标准中的第三类医疗器械。截至招股书披露日,全球有24款获批准商业化的主要经导管主动脉瓣置换产品,而中国有八款获批准商业化的经导管主动脉瓣置换产品,包括启明医疗的VenusA-Valve及VenusA-Plus、苏州杰成的J-Valve、微创心通医疗的VitaFlow及VitaFlowLiberty、沛嘉医疗的TaurusOne及TaurusElite及爱德华生命科学的SAPIEN3。
根据招股书援引佛若斯特沙利文资料,全球市场上,杰成医疗生产的J-Valve及JenaValveTechnology生产的Trilogy作为经导管主动脉瓣置换产品已将重度主动脉瓣返流治疗纳入适应症,并实现商业化。而Ken-Valve目前仅进展至确证性临床试验阶段。
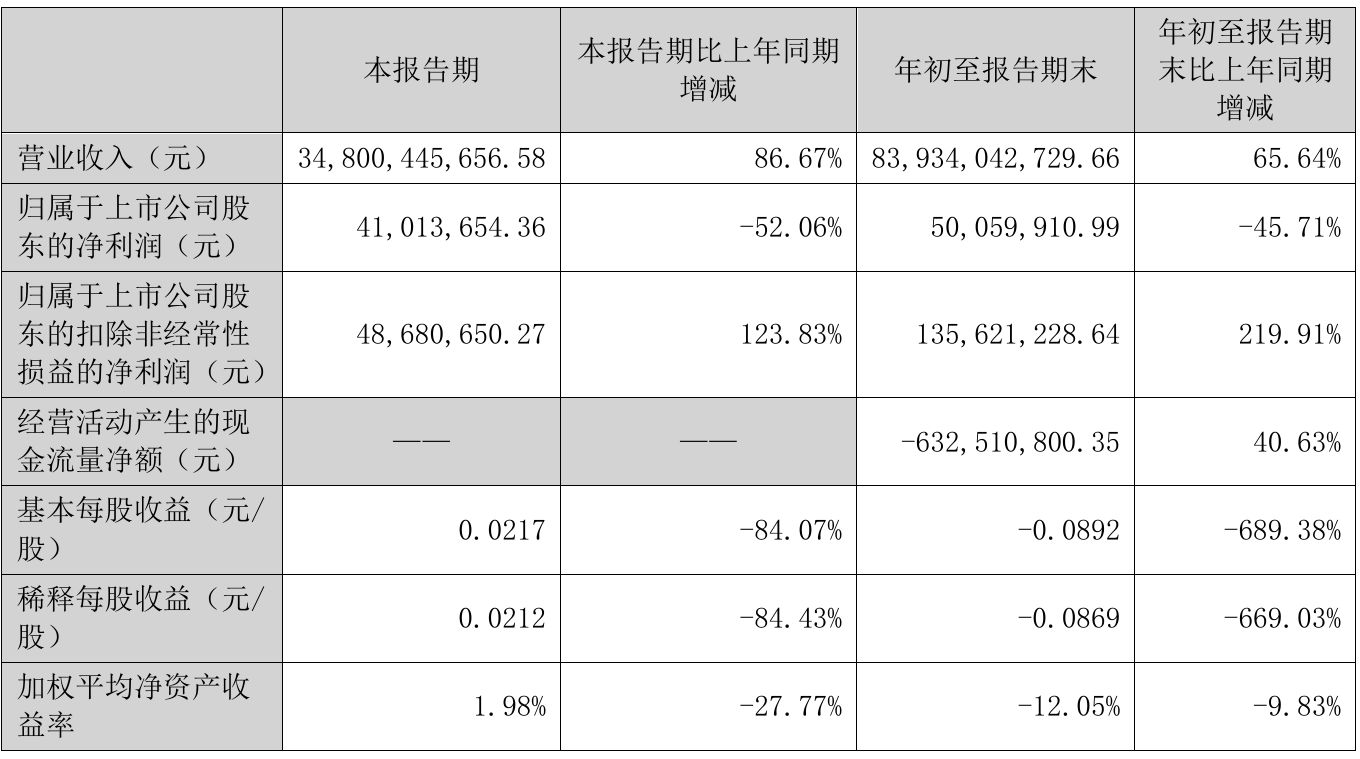
前三季度亏损4.21亿元
除两款核心产品外,健世科技还有8款分别针对瓣膜性心脏病和心力衰竭疾病的在研产品。针对瓣膜性心脏病中LuX-ValvePlus为经导管三尖瓣置换(TTVR)系统,预计将于2023年实现商业化。JensT-Clip为经导管三尖瓣修复(TTVr)系统,预计将于2025年实现商业化。KenFlex为经导管主动脉瓣置换(TAVR)系统,预计将于2025年上半年实现商业化。JensClip为经导管二尖瓣修复(TMVr)系统,预计将于2024年实现商业化。
针对心力衰竭疾病在研产品仅两款,分别为MicroFlux、AlginSysEndolnjex,均处于临床前阶段。MicroFlux为一款心房间隔造孔支架及输送系统,预计将于2024年实现商业化。AlginSysEndolnjex为一款心肌填充水凝胶及注入系统,预计将于2025年实现商业化。
大量的研发投入下健世科技连年亏损,并且亏损幅度不断扩大。2019-2020年及2021年前三季度,健世科技亏损金额分别为0.28亿元、3亿元和4.21亿元,同比扩大975.14%(2020年)、138.29%(2021年三季度)。同期研发开支分别为0.23亿元、1.71亿元和2.25亿元,研发投入为期间费用中占比最大的费用,且呈增加态势。
由于两款核心产品预计将于2023年和2024年才能实现商业化,健世科技目前的收入主要来自政府补助等其他收入及收益,短期盈利难。2019年、2020年及2021年三季度,健世科技其他收入及收益分别为180.7万元、307万元和986万元,经营活动所用现金流量净额分别为-1644.4万元、-4685.3万元和-9900.7万元、
高瓴为最大机构投资方
由于核心产品LuX-Valve研发进度领先且产品优势明显,作为一家创新的生物科技公司,健世科技在IPO前获得多方资本加持。2021年C轮融资后,公司估值达13.64亿美元。
此次IPO前,健世科技已获得高瓴资本、春华资本、辰德资本、Cormorant、华夏基金、DucklingFund,L.P.、中国人寿保险及人保等机构的投资。截至招股书披露日,董事会主席、控股股东吕世文及一致行动人控制注册资本2.11亿元,占公司股权约51.53%。高瓴资本持股4036.81万,持9.87%公司股权,为最大机构投资方。辰德资本和春华资本分别持有6.14%和6.09%的股份。
此外,2020年9月,为扩大心力衰竭业务部门,健世科技进行过一次重组,以股权转换等方式收购宁波迪创的100%股权。宁波迪创成立于2014年1月,专注于开发用于治疗心力衰竭的创新医疗器械。
值得注意的是,招股书显示宁波迪创为吕世文及一致行动人成立的公司。成立之初宁波麟沣、吕世文、李勤荣、锺伟及王莉分别拥有40%、30%、18%、6%及6%的股权,后经过股权转让及增资,在此次收购前,宁波迪创股权结构为吕世文持股55.33%、宁波麟沣持股34.67%和邬丹科持股10%。
资料来源:招股书
2020年9月,健世科技与吕世文、宁波麟沣及邬丹科以宁波迪创约6.67%股权对健世科技1%股权的比例进行股权置换,认购完成后一致行动人持有健世科技86.06%股权,邬丹科持有健世科技1.28%股权,其他股东持有12.66%股权。而健世科技持有宁波迪创100%股权。
招股书对此次重组提示风险,表示如果公司未能成功将最近收购的附属公司或未来目标公司整合到相关业务中,其收购后业绩和业务前景可能会受到不利影响。并进一步解释,受经济和竞争的影响,整合宁波迪创以实现与公司原有业务的协同效应具有不确定性。此外,未来公司收购产生的协同效应可能会因收购产生的成本、其他费用增加、经营亏损或业务的其他问题而被抵销。
您可能也感兴趣:
为您推荐
沪江材料将于1月18日上市北交所 公开发行价为18.68元/股
韦尔股份控股股东虞仁荣质押230万股 质押期限至2023年1月16日
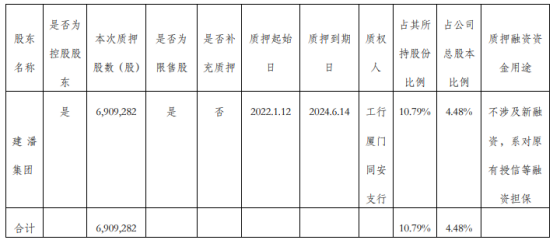
金牌厨柜控股股东建潘集团质押690.93万股 质押期限至2024年6月14日
排行
精彩推送
- 银行板块持续走强 多因素促估值修复
- 华谊腾讯娱乐:CEO袁海波失联不实,股票今日复牌
- 信息披露多次违规,华铁应急遭上交所监管警示
- 或有“戴帽”风险!獐子岛预告扣非净利润持续亏损
- 传祥生实业账户及旗下子公司股权被冻结,祥生方面回应银柿记者
- 进军换电的宁德时代,能否一统江湖?
- 趁着股价四连板“东风”,海量数据实控人忙着减持
- 长春高新连续跌停,控股股东部分质押突破此前平仓线,葛兰或...
- CRO高景气度持续,昭衍新药2021年净利预增,股价却跌跌不休
- 消息称字节跳动2021年或日均进账10.07亿元,但同比增速放缓
- 华润万象生活:拟收购南通长乐全部股权及江苏中南1%股权
- 报告期内因产品抽检不合格被通报 沃文特产品质量问题受关注
- 格兰尼冲刺创业板IPO存偿债风险
- 中恒宠物主要业绩增长稳健 IPO报告期内境外收入较高
- “哔嗨啤”啤酒被曝涉嫌传销,王老吉授权品牌惹火上身
- *ST华塑“抢发”年报保壳收问询,闪电并购的公司撑起8成营收...
- 天有教育上市招股书失效,去年前七个月总营收2.45亿元
- 小红书治理虚假种草 医美连锁品牌“广州曙光医学美容医院”...
- 小红书治理虚假种草 医美连锁品牌“海峡整形”被平台封禁
- 小红书治理虚假种草 日本美容品牌“佑天兰”被平台封禁
- 建发房产待偿还直接债务融资352亿元 拟发行中票部分募资用于并购
- 因为印章,真视通闹了小半年,终于恢复正常使用了!
- 长春高新连续两日跌停,股民人均浮亏13万,发生了啥?
- 瑞幸咖啡否认重回纳斯达克 业内人士称仍存诸多障碍需要“漫...
- 与“果链”深度捆绑的兴禾股份:需求下滑致营收净利双双骤减...
- 德盈控股对赌压力下曲折上市 营收增长乏力高度依赖B.Duck小黄鸭
- 小红书治理虚假种草 德国乳制品品牌“欧德堡”遭平台封禁
- 湖南鑫和医药虚开增值税发票1817万 被罚50万元
- 小红书治理虚假种草 网红民宿酒店安隅、渝舍印象、听花堂、I...
- 中科环保、BYD半导、工大科雅1月27日创业板首发上会
- 芯龙技术1月27日科创板首发上会
- 未按规定披露关联方及关联交易 ST华钰遭处罚
- V观财报|白云机场:2021年预亏约3.8亿-4.7亿
- V观财报|创力集团:董事长石华辉辞职
- 子公司失控后中嘉博创回函:不存在财务“大洗澡”
- V观财报|獐子岛:2021年净利同比预降39%-60%
- 年审报告存虚假记载!中天运被暂停债务融资工具相关业务
- 投诉量超6000条,新老IP交替明显!股价走低泡泡玛特如何破局?
- 净利润增速首次下探!保利发展频繁融资溢价拿地为哪般?
- 恒泰证券原营业部负责人“搞副业”,大连证监局对其出具警示函
- 14批次化妆品被检出禁用原料 涉及广州碧婷化妆品等企业
- 长春高新连续两日跌停 生长激素纳入集采价格或下降70%
- 小红书治理虚假种草 日本保温杯品牌“GERM格沵”遭平台封禁
- “韩束、一叶子”母公司上美集团冲击港交所 近三年营销开支...
- 百世集团因交通事故新增被执行人 执行标的127.74万元
- 权健新增3条被执行人信息 执行金额156.50万元
- 苏大维格实控人陈林森收监管函 敏感期交易自家股票
- 雅本化学收监管函 被问信披是否误导及配合股东减持
- 麦田房产经纪1天收2罚单 为禁止交易房屋提供经纪服务
- 当“织布机”变成“断魂刀”,一场万亿成交下的存量博弈
- 三安光电股价3连阴 海通证券安信证券高点唱多
- 足力健新增被执行信息 执行标的为128万元
- 任泽平与东吴证券属编外合作?以独立学者身份发表观点不代表...
- 华夏航空:副总裁崔新宇辞职
- 嘉化能源:牛瑛山辞去副总经理职务
- 盐湖股份去年净利预增90%-110% 股价今跌7.58%
- 提价效果不佳 生活用纸业持续承压 厂商大笔回购难解困境
- 方正证券去年净利预增50%-70% 股价今涨0.64%
- 盐津铺子实控人等增持仅完成25%就喊停 股价跌2.18%
- 博盈特焊募投项目或存“注水”发行人律师合伙人辞职后任公司董秘
- 写“差评”被判侵权考研机构续:一被告称其知乎账号是他人在用
- 高德联合清华大学发布报告显示:贫困地区经济民生因路而兴
- 联创股份跌13.98% 万联证券高位喊买入
- 1月19日(周三)港股沽空数据出炉 正荣地产沽空比率居首位
- 万达楼盘大门脱落,砸死代驾小哥
- 万人请辞策划冲上热搜一!哈利波特手游道歉,啥情况?
- 网红书店西西弗销售无3C认证儿童商品被罚
- ST起步说明变更会计师事务所相关情况
- 杜嘉班纳违法开除员工判赔36万元
- 网易旗下《哈利波特:魔法觉醒》手游因春节活动引争议,回应...
- 青客租房申请破产清算,此前未履行金额近3000万元
- 安徽建工开年三次成被执行人:去年累计至少4次被列为被执行人...
- 既然有周期,那就有盈亏!”猪茅”净利大滑坡,猪养的到底咋样?
- 小红书起诉4家涉虚假种草通告平台、MCN机构:索赔1000万
- 帝欧家居澄清:欧神诺仍为公司控股子公司
- 诚达药业登陆深交所创业板
- 紫燕食品冲击IPO:年营收超26亿华东贡献超7成,关联销售总额达16亿
- 瑞思教育,再无丰年?
- 三问森马:卖啥?谁卖?咋卖?
- 瑞幸否认重回纳斯达克上市传闻:报道不实
- 阿里文娱退出优酷股东,改由其子公司土豆网络全资持股
- 有赞被爆裁员,官方暂未回应
- 安踏品牌2021年零售金额同比增长25-30%,FILA“显疲态”连续...
- 得利斯诉Yolarno案获法官支持判决,有权追讨600万澳元收购预付款
- 生长激素纳入集采,“生长茅”长春高新闪崩跌停,安科生物大跌7%
- 转型初期多位高管来自竞争对手杉杉,后期业绩靠宁德时代一飞...
- 孩子王预计全年净利润1.96-2.35亿元,同比下滑40%-50%
- 特斯拉霸主地位不保?美银:2024年美国市占率仅为19%
- 两年未融资、扩张失序 钱大妈面临“囚徒困境”
- “女鞋第一股”告别女鞋业务,预亏超4亿的星期六还能好吗?
- 搭上NFT的快车 多次“跨界”的吉宏股份能走多远?
- 港股餐饮板块齐嗨 九毛九涨幅超6% 多家投行看好公司前景
- 永清环保净利预增超1倍 公司称双碳服务将成重点方向
- 伽玛刀进藏! 西部大棋局又拱一卒
- 百年人寿泉州本部营业区开展“苏垵养老院公益活动”
- 医疗版块遭遇黑天鹅,进入调整期
- 美股周三收跌 汇丰银行预计美股全年回报将十分微薄
- 今日上市:诚达药业
- 福安药业超1亿股权转让首期款未收回 研发进入“收获期”账面...
- 汉得信息会计核算调整致净利预增2倍 扣非连亏三季研发费不降...





 营业执照公示信息
营业执照公示信息